Comment se déroule une recherche clinique ?

Les recherches sur la personne peuvent avoir des objectifs très divers : le développement d’un nouveau médicament, d’un nouveau dispositif médical, la preuve des effets d’un complément alimentaire, la recherche des impacts sur la personne de certains comportements…
Chaque volontaire peut choisir une étude qui l’intéresse.
Un temps d'échange entre le volontaire et le médecin :
Tout d’abord l’investigateur (la personne qui dirige et surveille la recherche) va discuter avec le volontaire pour lui expliquer : les objectifs, l’organisation, les contraintes et les risques liés à la recherche.
Concrètement, il devra lui expliquer : combien il y aura de visites à l’hôpital, en cabinet de ville ou à domicile ; combien de temps va durer chaque visite ; quels sont les examens, les actes qui seront réalisés lors de ces visites ; ce qui se passera en cas de sortie de la recherche avant la fin.
Pour chaque intervention, le volontaire doit savoir comment elle va se dérouler, combien de temps elle va durer, quels seront ses effets, quels sont ses risques.
Par exemple :
Votre médecin investigateur effectuera une mesure des signes vitaux, comprenant le pouls, la tension artérielle, la fréquence respiratoire, les mesures de la température corporelle.
Aux visites 1 et 4, sera réalisé un Électrocardiogramme (ECG). C’est un enregistrement de l’activité électrique de votre cœur, Cet examen est rapide, il ne prend que quelques minutes ; il est indolore, non invasif et dénué de tout danger. On va placer à divers endroits sur votre torse des électrodes adhésives qui vont enregistrer l’activité de votre cœur.
L’ensemble des interventions et des visites est souvent représenté sous forme de tableau, exemple :
| Visite 1 : Jour 0 | Visite 2 : Jour 15 | Visite 3 jour : 30 | Visite 4 : J45 |
Signature du consentement | X |
|
|
|
Examen clinique | X | X | X | X |
ECG | X |
|
| X |
Prélèvement sanguin 5 mL | X | X | X | X |
Echographie cardiaque | X |
|
| X |
Traitement | X | X | X | X |
La création de groupes d'étude : La randomisation
Si la recherche porte sur un produit, il est possible que deux ou plusieurs groupes de personnes soient constitués pour effectuer des comparaisons. Un médicament peut être comparé à un placebo ou à un autre médicament qui est la référence actuelle de traitement pour la maladie. Le placebo est fabriqué spécifiquement pour ressembler au médicament testé, mais il ne contient pas de substance active. Quand on compare les effets d’un médicament contre un placebo, on élimine tout ce qui peut se produire qui serait dû, notamment au fait que la personne pense être traitée, et l’on évalue donc l’efficacité et la sécurité objectives du nouveau médicament. Il arrive que des personnes qui reçoivent le placebo d’un médicament, c’est à dire un produit qui ne contient aucune substance active, aient des effets secondaires de ce médicament. C’est ce que l’on appelle l’effet nocebo.
Pour que la différence que l’on va observer soit due aux effets du médicament, il faut que les deux groupes de personnes soient comparables. Si par exemple, l’on a un groupe avec des personnes plus âgées que l’autre, alors la fréquence plus importante d’un effet secondaire peut être due à l’âge et pas au médicament.
Pour assurer la comparabilité des groupes, il faut faire une randomisation, c’est à dire que le traitement pour chaque nouveau volontaire sera tiré au sort.
En aveugle, les volontaires ne sauront pas s’ils prennent le médicament ou le placebo. Dans la majorité des cas, les recherches comparatives sont organisées en double aveugle : l’investigateur et toute son équipe ne savent pas non plus quel est le produit administré au volontaire.
Souvent un schéma est présenté pour expliquer cela :
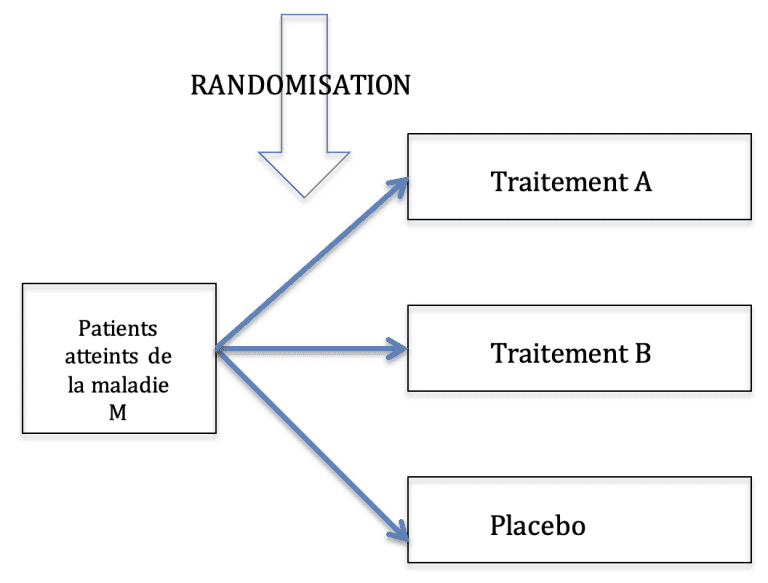
La collecte des résultats :
Tout au long de la recherche l’investigateur va collecter des données de santé. Cette période peut durer quelques jours pour une recherche sur un cosmétique par exemple, mais également plusieurs années pour des recherches sur des molécules très complexes.
Les volontaires sont des acteurs principaux dans cette phase active de la recherche et à travers notre association nous souhaitons leur redonner une importance toute particulière. Notamment en leur permettant de mieux connaître et comprendre la recherche clinique ainsi que les enjeux qu’elle représente.
Quelques notes pratiques si vous souhaitez participer à une recherche :
A la fin de l’entretien avec l’investigateur, vous devez avoir un délai de réflexion. Ce délai va vous permettre de relire la note d’information, si vous le souhaitez de poser des questions à l’investigateur, de réfléchir et de prendre votre décision.
Ensuite si vous voulez participer à la recherche, vous devez signer un consentement. Pour les recherches de catégorie 2 (à risques et contraintes minimes) le consentement doit être juste exprimé ; il n’est pas obligatoirement écrit, cela peut être un simple clic en ligne, à condition que votre identité puisse être contrôlée. Pour les recherches non interventionnelles (catégorie 3) vous serez informé et si vous ne voulez pas participer à la recherche, vous devrez exprimer votre opposition. A tout moment, vous pouvez poser des questions et si vous ne vous sentez pas en mesure de continuer, vous pouvez retirer votre consentement et arrêter la recherche.
Si vous participez à une recherche sur le traitement de votre maladie, celle-ci peut vous apporter une meilleure connaissance de la pathologie en général. De plus, le suivi très rigoureux et comprenant de nombreux examens, vous permettra de mieux connaître votre état de santé et son évolution.
